
分析 (1)鋁、鐵、銅中,銅導電能力最強,鋁次之,鐵導電能力最差,并且鐵容易生銹;
現實生活中應用最廣泛的金屬是鋼鐵;
鋁具有很好的抗腐蝕性能,是因為通常情況下,鋁能和空氣中的氧氣反應生成一層致密的氧化鋁薄膜,對里面的鋁制品起到保護作用;
(2)化合物中元素化合價代數和為零;
化學反應前后,元素的種類不變,原子的種類、總個數和質量不變;
根據反應物、生成物、反應條件及其質量守恒定律可以書寫反應的化學方程式.
解答 解:(1)①常作為導線的金屬是鋁和銅,應用最廣泛的金屬是鐵.
故填:鋁和銅;鐵.
②鋁具有很好的抗腐蝕性能,原因是通常情況下,鋁能和空氣中的氧氣反應生成一層致密的氧化鋁薄膜,對里面的鋁制品起到保護作用,反應的化學方程式為:4Al+3O2═2Al2O3.
故填:4Al+3O2═2Al2O3.
(2)①設FeTiO3中鈦元素的化合價為x,
根據題意有:(+2)+x+(-2)×3=0,
x=+4,
故填:+4.
②由2FeTiO3+6C+7Cl2 $\frac{\underline{\;高溫\;}}{\;}$ 2TiCl4+2X+6CO可知,反應前有2個鐵原子,反應后應該有2個,包含在2X中,反應前后都是1個鈦原子,反應前后都是6個氧原子,反應前后都是6個碳原子,反應前有14個氯原子,反應后應該有14個氯原子,其中6個包含在2X中,因此X的化學式為FeCl3.
故填:FeCl3.
③鎂與TiCl4反應生成金屬鈦和氯化鎂,反應的化學方程式為:TiCl4+2Mg$\frac{\underline{\;高溫\;}}{\;}$Ti+2MgCl2.
故填:TiCl4+2Mg$\frac{\underline{\;高溫\;}}{\;}$Ti+2MgCl2.
點評 本題主要考查物質的性質,解答時要根據各種物質的性質,結合各方面條件進行分析、判斷,從而得出正確的結論.


科目:初中化學 來源: 題型:選擇題
| A. | 2NaOH+H2SO4═Na2SO2+2H2↑+O2↑ | B. | 2Ag+2HCl═2AgCl↓+H2↑ | ||
| C. | 6HCl+Fe2O3═3H2O+2FeCl3 | D. | 3KCl+Al(NO3)3═3KNO3+AlCl3 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 選項 | 實驗目的 | 實驗方法 |
| A | 除去粗鹽中的難溶性雜質 | 將粗鹽研碎、溶解、蒸發 |
| B | 除去鐵制品上的鐵銹 | 將鐵制品長時間浸泡在足量的稀硫酸中 |
| C | 鑒別石灰水和NaOH溶液 | 加入適量的稀鹽酸 |
| D | 檢驗某礦石中是否含碳酸鹽 | 加入適量的稀鹽酸,若產生氣體再將氣體通入澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
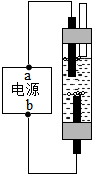 2017年“世界水日”的宣傳主題是“Wastewater”(廢水),如何將廢水轉化為有用之水是各國研究的重大課題.
2017年“世界水日”的宣傳主題是“Wastewater”(廢水),如何將廢水轉化為有用之水是各國研究的重大課題.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
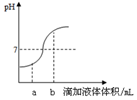 如圖是鹽酸和氫氧化鈣溶液用滴加方式反應時,溶液pH隨滴入溶液體積變化的曲線.下列有關說法正確的是( )
如圖是鹽酸和氫氧化鈣溶液用滴加方式反應時,溶液pH隨滴入溶液體積變化的曲線.下列有關說法正確的是( )| A. | 該圖象表示的是將稀鹽酸滴入氫氧化鈣溶液中 | |
| B. | 當滴入溶液的體積為amL時,所得溶液中的溶質只有CaCl2 | |
| C. | 滴入溶液體積為bmL時,再加幾滴酚酞試液溶液呈紅色 | |
| D. | 恰好完全反應后溶液中存在的粒子只有Ca2+和Cl-離子 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
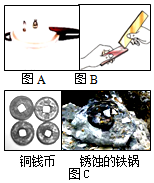 金屬材料在生活、生產中應用十分廣泛.
金屬材料在生活、生產中應用十分廣泛.查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
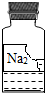 實驗室有一瓶無色溶液,標簽變得殘缺不全(如圖所示),同學們設計以下方案探究該溶液的成分
實驗室有一瓶無色溶液,標簽變得殘缺不全(如圖所示),同學們設計以下方案探究該溶液的成分| 實驗步驟 | 實驗現象與化學方程式 | 實驗結論 |
| 方案一:取少量待測溶液于一支試管中,向其中滴加無色酚酞試液(提示:硫酸鈉溶液為中性) | 實驗現象:溶液變為紅色. | 猜想二正確 |
| 方案二:取少量待測液于一支試管中,向其中滴加稀鹽酸; | 實驗現象:溶液中有氣泡產生.化學方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑. | |
| 方案三:取少量待測溶液于一支試管中,向其中滴加氯化鋇溶液 | 實驗現象:產生白色沉淀. |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
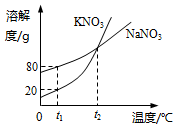
| A. | t1℃時,兩物質的溶液溶質質量分數一定不等 | |
| B. | t1℃時,50g水里加入15g KNO3固體,充分溶解,得到60g溶液 | |
| C. | t1℃時,兩物質飽和溶液升溫到t2℃后,溶質質量分數:NaNO3=KNO3 | |
| D. | 兩種物質飽和溶液從t2℃降溫到t1℃時,析出晶體的質量:KNO3>NaNO3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com