


科目:初中化學 來源: 題型:
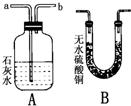
 32、某學校的探究性學習小組發現,銅綠[Cu2(OH)2CO3]受熱分解后,除生成CO2和水蒸氣外,試管中還有一些黑色粉末狀固體.他們通過實驗探究,分析黑色固體的組成,并驗證產生的氣體.請填空:
32、某學校的探究性學習小組發現,銅綠[Cu2(OH)2CO3]受熱分解后,除生成CO2和水蒸氣外,試管中還有一些黑色粉末狀固體.他們通過實驗探究,分析黑色固體的組成,并驗證產生的氣體.請填空:查看答案和解析>>
科目:初中化學 來源: 題型:
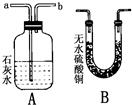 ,則猜想c成立.
,則猜想c成立.查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源:2007年山東省東營市中考化學模擬試卷(解析版) 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com