
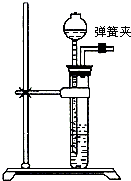
 31、化學實驗小組在實驗室制備氫氣時,發現沒有鋅粒或鐵屑,僅有一些碎鋁片.根據有關資料提示,他們將鋁片放入燒堿溶液中,除去表面的氧化膜(Al2O3),洗凈后用于制取氫氣.
31、化學實驗小組在實驗室制備氫氣時,發現沒有鋅粒或鐵屑,僅有一些碎鋁片.根據有關資料提示,他們將鋁片放入燒堿溶液中,除去表面的氧化膜(Al2O3),洗凈后用于制取氫氣.

 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
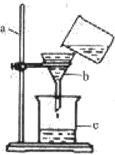 某化學實驗小組在實驗室中對一燒杯渾濁的河水進行了簡單凈化.回答下列問題:
某化學實驗小組在實驗室中對一燒杯渾濁的河水進行了簡單凈化.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com