分析:(1)本題實驗設計比較新穎,并且能夠很好的防止污染環境,能很容易的控制可變條件,完成對比試驗;但是考查的仍然是燃燒的條件,我們在解答本題時要注意從白磷燃燒的現象來分析解答,同時本題還涉及到了與物理中的氣體壓強方面的問題,解答時要注意聯系物理知識.
(2)①根據物質中某元素的質量分數=
×100%,可求出理論含氮質量分數,②根據某物質的純度=
×100%進行解答.
解答:解:(1)根據實驗裝置,結合白磷的著火點較低,而紅磷的著火點較高,不易達到,所以我們可以觀察到試管中的白磷燃燒,而紅磷和水中的白磷不會燃燒,同時由于溫度升高使氣體壓強增大,而使球變大,等燃燒完成后,由于消耗了氧氣而使氣球變小;
故答案為:只有試管A中的白磷燃燒,發光放熱,產生白煙,氣球先變大后變小.燒杯水中的白磷熔化,紅磷沒有變化;
(2)本實驗是在密閉的裝置中完成的可以避免產生的白煙污染空氣,同時又做了對照實驗,一目了然的得出了燃燒的條件,故答案為:保護環境,控制變量
(3)白磷燃燒要消耗氧氣,由于本裝置是密閉的,當把試管倒放入水中時,會由于試管中氧氣被消耗,而使壓強小于外界大氣壓,又因為氧氣約占空氣體積的五分之一,而使水大約進入試管的五分之一處;
故本案為:試管中液面上升;白磷燃燒消耗了氧氣,使瓶內壓強變小,外界大氣壓把水壓入試管中
(2)①碳酸氫銨中氮元素的質量分數=
×100%=17.7%;
②這種氮肥的純度=
×100%=94.9%.
故答案為:①17.7% ②94.9%

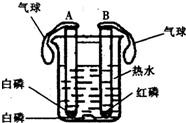 (1)如圖為某學生設計的探究可燃物燃燒條件的實驗,請回答:
(1)如圖為某學生設計的探究可燃物燃燒條件的實驗,請回答: