學習氫氧化鈉的性質時,老師為了讓同學們看到CO
2與氫氧化鈉反應有明顯現象,設計了演示實驗:給集滿CO
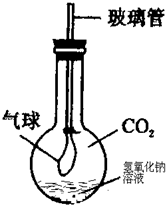
2的燒瓶中加入濃的氫氧化鈉溶液,然后迅速蓋上并塞緊帶有玻璃管的膠塞,玻璃管下端套有一氣球(如圖).振蕩燒瓶后,可看到的現象是
氣球膨脹
氣球膨脹
原因是
二氧化碳和氫氧化鈉溶液反應生成碳酸鈉和水,反應后燒瓶內的壓強變小
二氧化碳和氫氧化鈉溶液反應生成碳酸鈉和水,反應后燒瓶內的壓強變小
.
寫出該反應的化學方程式:
CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
可是細心的小明同學發現,經老師用力振蕩后燒瓶內液體呈白色渾濁!好學的小明同學很想知道白色渾濁是什么物質,為此他進行了以下的探究活動:
【查閱資料】(1)在氫氧化鈉溶液中通入過量的二氧化碳會生成碳酸氫鈉,該反應的化學方程式為
NaOH+CO
2+H
2O═NaHCO
3;
(2)常溫下,NaHCO
3在水中的溶解度比Na
2CO
3小.Na
2CO
3過飽和后也會結晶析出.
(3)Ca(HCO
3)
2 可溶于水.
【猜想】猜想一:該白色渾濁物中只有Na
2CO
3;
猜想二:該白色渾濁物中只有NaHCO
3;
猜想三:該白色渾濁物中可能有
Na2CO3和NaHCO3
Na2CO3和NaHCO3
.
【實驗探究】
設計實驗驗證猜想:小明同學根據老師的提示將該渾濁液體加水攪拌后發現白色渾濁消失形成無色溶液!這些神奇的變化讓小明更加好奇,他于是又設計了以下實驗來驗證其猜想:
| 實驗步驟 |
實驗現象 |
結論 |
| ①取少量加水后形成的無色溶液,加入過量CaCl2溶液,靜置. |
出現白色沉淀(或無明顯現象) 出現白色沉淀(或無明顯現象) |
該溶液中 Na2CO3(或沒有Na2CO3) Na2CO3(或沒有Na2CO3) |
| ②再取步驟①的上層清液,加入 稀鹽酸 稀鹽酸 . |
有氣泡冒出(或無明顯現象) 有氣泡冒出(或無明顯現象) |
證明該溶液中 NaHCO3(或沒有NaHCO3) NaHCO3(或沒有NaHCO3) |
小明通過努力終于明白了二氧化碳與氫氧化鈉溶液反應后液體出現白色渾濁的原因.請你通過以上實驗現象分析說出小明完成本實驗的最后結論是:猜想
三
三
正確.
