
 36、在高效復(fù)習(xí)課堂中,同學(xué)們利用“硫酸、硝酸鋇、氫氧化鈉、碳酸鉀”四種物質(zhì)的溶液對(duì)“復(fù)分解反應(yīng)發(fā)生的條件”進(jìn)行再探究.
36、在高效復(fù)習(xí)課堂中,同學(xué)們利用“硫酸、硝酸鋇、氫氧化鈉、碳酸鉀”四種物質(zhì)的溶液對(duì)“復(fù)分解反應(yīng)發(fā)生的條件”進(jìn)行再探究.| 溶液中可能含有的離子 | 設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證 | ||
| 實(shí)驗(yàn)步驟 | 現(xiàn)象 | 結(jié)論 | |
| 溶液中可能含有的離子 | 設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證(實(shí)驗(yàn)步驟、現(xiàn)象及對(duì)應(yīng)的結(jié)論) |
| 可能性一:Ba2+(同時(shí)答兩種或兩種以上離子的不得分,下同.) | 取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有Ba2+. |
| 可能性二:SO42- | 取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有SO42-;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有SO42-. |
| 可能性三:Ba2+或SO42- | 取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+,不含有SO42-.(若沒有出現(xiàn)白色沉淀,必須驗(yàn)證SO42-)(其他答案合理給分.) |
| 溶液中可能含有的離子 | 設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證(實(shí)驗(yàn)步驟、現(xiàn)象及對(duì)應(yīng)的結(jié)論) |
| 可能性一:Ba2+(同時(shí)答兩種或兩種以上離子的不得分,下同.) | 取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有Ba2+. |
| 可能性二:SO42- | 取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有SO42-;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有SO42-. |
| 可能性三:Ba2+或SO42- | 取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+,不含有SO42-.(若沒有出現(xiàn)白色沉淀,必須驗(yàn)證SO42-)(其他答案合理給分.) |
| 溶液中可能含有的離子 | 設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證(實(shí)驗(yàn)步驟、現(xiàn)象及對(duì)應(yīng)的結(jié)論) |
| 可能性一:Ba2+(同時(shí)答兩種或兩種以上離子的不得分,下同.) | 取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有Ba2+. |
| 可能性二:SO42- | 取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有SO42-;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有SO42-. |
| 可能性三:Ba2+或SO42- | 取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+,不含有SO42-.(若沒有出現(xiàn)白色沉淀,必須驗(yàn)證SO42-)(其他答案合理給分.) |


 閱讀快車系列答案
閱讀快車系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:初中化學(xué) 來源: 題型:閱讀理解

| 溶液中可能含有的離子 | 設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證(實(shí)驗(yàn)步驟、現(xiàn)象及對(duì)應(yīng)的結(jié)論) |
可能性一:Ba2+ 可能性二:SO42- 可能性三:Ba2+或SO42- 可能性一:Ba2+ 可能性二:SO42- 可能性三:Ba2+或SO42- | ①取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有Ba2+., ②取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有SO42-;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有SO42-. ③取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+,不含有SO42-. ①取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有Ba2+., ②取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有SO42-;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有SO42-. ③取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現(xiàn)白色沉淀,則說明上述溶液中含有Ba2+,不含有SO42-. |
查看答案和解析>>
科目:初中化學(xué) 來源: 題型:閱讀理解

| 溶液中可能含有的離子 | 設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證(實(shí)驗(yàn)步驟、現(xiàn)象及對(duì)應(yīng)的結(jié)論) |
可能含SO42- 可能含SO42- |
取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現(xiàn)白色沉淀,則說明含有SO42-;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有SO42-. 取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現(xiàn)白色沉淀,則說明含有SO42-;若沒有出現(xiàn)白色沉淀,則說明上述溶液中不含有SO42-. |
查看答案和解析>>
科目:初中化學(xué) 來源: 題型:閱讀理解
| 時(shí)間/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水質(zhì)量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
| 溶液中可能含有的離子 | 設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證(實(shí)驗(yàn)步驟、現(xiàn)象及對(duì)應(yīng)的結(jié)論) |
SO42- SO42- |
取少量濾液,加入硝酸鋇溶液,若有白色沉淀產(chǎn)生,說明溶液中含有SO42-;若無白色沉淀產(chǎn)生,說明溶液中不含有SO42-. 取少量濾液,加入硝酸鋇溶液,若有白色沉淀產(chǎn)生,說明溶液中含有SO42-;若無白色沉淀產(chǎn)生,說明溶液中不含有SO42-. |
查看答案和解析>>
科目:初中化學(xué) 來源: 題型:
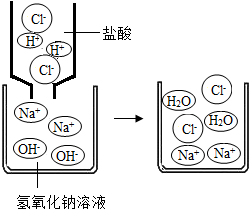 在高效復(fù)習(xí)課堂中,同學(xué)們利用“硝酸、氯化鋇、氫氧化鉀、硫酸鎂”四種物質(zhì)的溶液對(duì)“復(fù)分解反應(yīng)發(fā)生的條件”進(jìn)行再探究.
在高效復(fù)習(xí)課堂中,同學(xué)們利用“硝酸、氯化鋇、氫氧化鉀、硫酸鎂”四種物質(zhì)的溶液對(duì)“復(fù)分解反應(yīng)發(fā)生的條件”進(jìn)行再探究.查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com