
【題目】有Cu2(OH)2CO3[Mr=222]與Cu的混合物25.4g,在空氣中加熱一段時間,得剩余固體23.1g,向該固體中加入300.0g9.8%的稀硫酸,固體完全溶解,測得反應過程中實際消耗9.8%的稀硫酸250.0g。下列說法正確的是
A. 剩余固體為純凈物
B. 上述加熱過程中共生成H2O和CO2的質量為2.3g
C. 原混合物中Cu2(OH)2CO3與Cu的質量比為111:16
D. 最終所得溶液質量為318.7g
【答案】C
【解析】
剩余固體中加入稀硫酸之后固體完全溶解,說明剩余固體中不含有銅單質。
設剩余固體中銅元素的質量為x
則有Cu——H2SO4
64 98
x 250g![]() 9.8%
9.8%
x=16g
設剩余固體中氧化銅的質量為y,堿式碳酸銅的質量為z
則有y+z=23.1g,![]()
解得y=12g,z=11.1g
設原固體中銅的質量為p,堿式碳酸銅的質量為q
則有p+q=25.4g,![]()
解得p=3.2g,q=22.2g
所以分解的堿式碳酸銅的質量為22.2g-11.1g=11.1g
根據分解的堿式碳酸銅的質量可求得生成的水和二氧化碳的質量
Cu2(OH)2CO3——H2O+CO2
222 62
11.1g 3.1g
所以生成的水和二氧化碳的質量為3.1g
剩余固體中堿式碳酸銅和硫酸反應生成的二氧化碳的質量
Cu2(OH)2CO3——CO2
222 44
11.1g 2.2g
A、剩余的固體混合物中含有堿式碳酸銅和氧化銅兩種物質,屬于混合物,錯誤;B、上述加熱過程共生成水和二氧化碳的質量為3.1g,錯誤;C、原混合物中堿式碳酸銅與銅的質量比是22.2:3.2=111:16,正確;D、剩余固體中堿式碳酸銅和硫酸反應生成的二氧化碳的質量為2.2g,則所得溶液的質量為300g+23.1g-2.2g=320.9g。


科目:初中化學 來源: 題型:
【題目】a、b、c三種固體物質的溶解度曲線如圖所示:

(1)P點表示___________________________________ 。
(2)將接近飽和的c溶液變為飽和溶液,可采用____________的方法(寫出一種)。
(3)t2℃時,將30g的a物質加入到50g水中充分攪拌,所得溶液質量為___________g。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某化學實驗室從含少量硝酸鋅的硝酸銀廢液中提取貴金屬Ag,其主要操作流程如下:
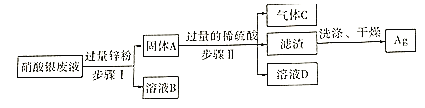
(1) 物體A的成分有___________ ;
(2) 步驟Ⅰ中發生的化學反應方程式_________________________;
(3) 步驟Ⅰ、Ⅱ共同的實驗操作名稱是___________,若往溶液D中加入適量的氧化鋅,可得到只含一種溶質的溶液,則發生反應的化學方程式為_____________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖為某品牌過氧化氫溶液說明書,,用該品牌過氧化氫溶液配制600g10%的過氧化氫溶液用于消毒,請回答下列問題:

(1)溶質(H2O2)的相對分子質量_____________。
(2)溶質(H2O2)中氫、氧元素質量比為_____________。
(3)600g10%的過氧化氫溶液中含有_____________g溶質,配置時需要加入__________g水進行稀釋。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖中A~D為四種不同類別的物質,D可用作某些氣體的干燥劑,廣泛用于制取肥皂,以及石油、造紙等工業.“—”表示相連的物質能發生反應,“→”表示一種物質能生成另一種物質(部分反應物、生成物和反應條件已略去)。
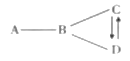
通過推理和判斷回答下列問題:
(1)寫出A的化學式_______;A與B能發生反應的原因是_____。
(2)B與D反應的實質是______。
(3)寫出D→C的化學反應方程式_______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖為某些物質間的轉化關系。甲、乙、丙均為氣體,乙有刺激性氣味,丁是應用最廣泛的金屬。A是大理石的主要成分,G是一種化肥,H為紅棕色固體。部分反應物和生成物已略去。
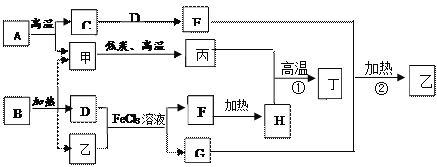
(1)化學式:B __ ,F __。
(2)自然界中,甲和D反應產生一種供呼吸的氣體,該反應名稱為______。
(3)反應①、②的化學方程式:①____ ;②____。
(4)由反應②可知,在農業上施用G時應注意______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某研究性學習小組欲測定石灰石中碳酸鈣的質量分數,采用的方法如下:取該石灰石樣品5g,把 60g稀鹽酸分四次加入,實驗過程所得數據如下表(已知石灰石樣品中含有的雜質 不溶于水,也不與稀鹽酸反應)。根據實驗數據計算:
實驗次數 | 1 | 2 | 3 | 4 |
加入稀鹽酸的質量/g | 15 | 15 | 15 | 15 |
剩余固體的質量/g | 3.50 | 2.00 | 0.75 | 0.75 |
(1)石灰石樣品中碳酸鈣的質量分數為_____。
(2)求原 60g 稀鹽酸中溶質質量分數(要求書寫計算過程)__________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】凡是有元素化合價發生變化的化學反應都屬于氧化還原反應,下列不屬于氧化還原反應的是( )
A. Zn+H2SO4==ZnSO4+H2↑ B. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
C. 2NaOH + H2SO4==Na2SO4+2H2O D. 4P+5O2![]() 2P2O5
2P2O5
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com