
分析:首先搞清:①石灰石的主要成分是CaCO3;②混合物減少的質量即CaCO3跟鹽酸反應,生成CO2的質量;③根據化學方程式中CaCO3與鹽酸、CO2的質量關系可計算出CaCO3的質量和用去鹽酸的質量,再根據密度即可求出鹽酸的體積。
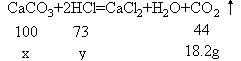 解:設參加反應的CaCO3的質量為xg,鹽酸溶液中的溶質質量為y。
解:設參加反應的CaCO3的質量為xg,鹽酸溶液中的溶質質量為y。
100∶44=x∶18.2g x=41.4g
 73∶44 = y∶18.2g y=30.2g
73∶44 = y∶18.2g y=30.2g
消耗鹽酸=30.2g÷20%=151g
20%鹽酸的體積=151/1.10=137.3(mL)答:略。
科目:初中化學 來源: 題型:
| 第一次 | 第二次 | 第三次 | |
| 所取石灰石合金的質量/g | 25 | 25 | 50 |
| 所用稀鹽酸的質量/g | 120 | 160 | 100 |
| 二氧化碳的質量/g | 9.9 | 9.9 | 9.9 |
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
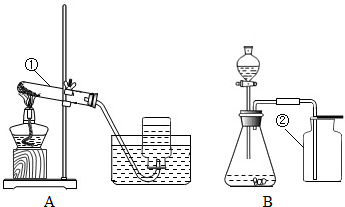
| 實驗步驟 | 實驗現象 |
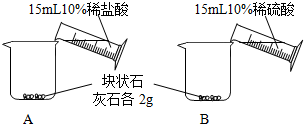 |
A中不斷產生氣泡,固體逐漸減少,有少量固體剩余. B中開始有少量氣泡產生,反應很快停止. |
| 實驗步驟 | 實驗現象 |
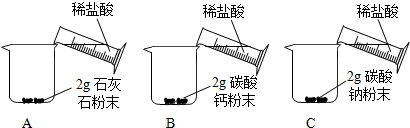 |
A中迅速產生大量氣泡,固體很快減少,有少量固體剩余. B、C中都迅速產生大量氣泡,固體很快消失. |
查看答案和解析>>
科目:初中化學 來源: 題型:
我市北部山區盛產石灰石,石灰石的主要成分是碳酸鈣。
(1)實驗室中常用石灰石制取二氧化碳,化學的反應方程式為 ;
其中碳酸鈣中鈣元素的質量分數為 。
(2)某校課外活動小組為了解石灰石資源的品質,對當地石材進行化學分析:取12.5g石灰石顆粒樣品,置于燒杯中并加入足量稀鹽酸,充分反應后稱得混合物的總質量減少了4.4g。則該石灰石中含碳酸鈣的質量分數是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com