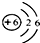解:(1)“低碳生活”就是減少CO
2的排放量;
(2)A、因碳的偏旁為“石”,則碳元素為非金屬元素,故A說法正確;
B、由信息可知,碳原子的質子數為6,故B說法正確;
C、碳原子的質子數為6,則原子結構中最外層電子數應為4,故C說法錯誤;
D、由信息可知,碳原子的相對原子質量為12.01,故D說法正確;
(3)①步驟III中存在二氧化碳氣體,二氧化碳不具備酸性,所以紙花不會變紅;步驟IV中紙花噴水后放入盛有二氧化碳的集氣瓶,則水與二氧化碳會生成碳酸,碳酸會使石蕊變紅,所以紙花變紅;
②步驟I中,醋酸顯酸性,能使紙花變紅.說明了酸能使紫色石蕊變紅,步驟Ⅱ中向紙花上噴水,紙花不變色,說明了水不能使紫色石蕊變紅;
③該同學進行四組對比實驗的目的是證明使紫色石蕊變紅的不是二氧化碳本身,而是由二氧化碳與水反應生成的碳酸;
④在該實驗中二氧化碳與水化合生成了碳酸,反應的方程式是:CO
2+H
2O=H
2CO
3;
(4)解:設需要碳的質量至少為x.
C+2CuO

2Cu+CO
2↑
12 160
x 80g
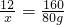
解得:x=6g
故答為:(1)CO
2; (2)C;(3)①紙花不變紅;紙花變紅;②說明了酸能使紫色石蕊變紅,而水不能使紫色石蕊變紅;③證明使紫色石蕊變紅的不是二氧化碳本身,而是由二氧化碳與水反應生成的碳酸; ④CO
2+H
2O=H
2CO
3;(4)需要碳的質量至少為6g.
分析:(1)“低碳生活”就是減少二氧化碳的排放量;
(2)根據元素周期表中的一個小格中的信息可知元素的名稱、元素符號、質子數、相對原子質量等來解答即可;
(3)依據石蕊遇酸性溶液會變紅以及二氧化碳溶于水會生成碳酸等知識結合各對比實驗的情況分析解決即可;
(4)根據碳與氧化銅的反應,由氧化銅的質量求出碳的質量.
點評:此題考查了石蕊的特點以及二氧化碳與水的反應,解題的關鍵是分清各對比實驗的目的以及相關的化學反應,屬于常規實驗考查題.

 為元素周期表中的一格,下列說法不正確的是______(填標號).
為元素周期表中的一格,下列說法不正確的是______(填標號).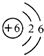 ;
;
 2Cu+CO2↑
2Cu+CO2↑ 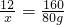 解得:x=6g
解得:x=6g 

 優生樂園系列答案
優生樂園系列答案 碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容.
碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容. 碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容.
碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容.
 碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容.
碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容. D.碳的相對原子質量為12.01
D.碳的相對原子質量為12.01
 碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容.
碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容.