(2009?朝陽)小慧同學在一次實驗中誤把高錳酸鉀當成了二氧化錳加入氯酸鉀中,加熱時,氯酸鉀的分解速率明顯加快.于是她驚奇地告訴同學小華:高錳酸鉀也可以作為氯酸鉀分解的催化劑.小華同學經過思考后,認為小慧同學得出的結論不科學.
(1)小華的理由是:______.
(2)如何證明高錳酸鉀不是氯酸鉀分解的催化劑:______.
(3)高錳酸鉀能加快氯酸鉀分解速率的原因是:______.
【答案】
分析:題干中關于實驗的敘述特別強調了誤把高錳酸鉀當成二氧化錳使用,加熱時,氯酸鉀的分解速率明顯加快,從現象上來看,好像是高錳酸鉀為該反應的催化劑,值就要求我們從實質的角度進行分析.平時在實驗和訓練中也要注意這種現象與本質之間的關系.
解答:解:由于高錳酸鉀在加熱時能夠發生分解:2KMnO
4 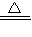
K
2MnO
4+MnO
2+O
2↑.這樣在氯酸鉀在受熱時高錳酸鉀分解出的MnO
2就能夠對氯酸鉀的分解起到催化的作用.2KClO
3 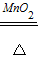
2KCl+3O
2↑這個過程中高錳酸鉀轉化為二氧化錳的等物質,其中的二氧化錳改變了氯酸鉀的分解速率,所以作催化劑的是二氧化錳,而非高錳酸鉀.從概念的角度,催化劑是質量和化學性質都不改變的物質,在這里,高錳酸鉀分解了,那么本身的化學性質改變,自身分解了,質量當然也就發生了改變,即高錳酸鉀在反應前后質量和化學性質都發生了改變.所以高錳酸鉀不是該反應的催化劑.
故答案:
(1)未驗證反應前后高錳酸鉀的質量和化學性質是否改變
(2)單獨加熱KMnO
4能產生O
2,說明KMnO
4不是催化劑
(3)因為高錳酸鉀受熱分解生成錳酸鉀二氧化錳和氧氣,二氧化錳對氯酸鉀的分解有催化作用,所以高錳酸鉀能加快氯酸鉀分解的速率.
點評:在回答問題時,一定要緊扣問題,說最實質的內容.如回答高錳酸鉀不是該反應催化劑一定要強調概念有關的質量和化學性質的改變,而不必要說明到底生成具體什么物質.也就是構建與概念等有關的橋梁.

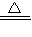 K2MnO4+MnO2+O2↑.這樣在氯酸鉀在受熱時高錳酸鉀分解出的MnO2就能夠對氯酸鉀的分解起到催化的作用.2KClO3
K2MnO4+MnO2+O2↑.這樣在氯酸鉀在受熱時高錳酸鉀分解出的MnO2就能夠對氯酸鉀的分解起到催化的作用.2KClO3 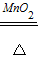 2KCl+3O2↑這個過程中高錳酸鉀轉化為二氧化錳的等物質,其中的二氧化錳改變了氯酸鉀的分解速率,所以作催化劑的是二氧化錳,而非高錳酸鉀.從概念的角度,催化劑是質量和化學性質都不改變的物質,在這里,高錳酸鉀分解了,那么本身的化學性質改變,自身分解了,質量當然也就發生了改變,即高錳酸鉀在反應前后質量和化學性質都發生了改變.所以高錳酸鉀不是該反應的催化劑.
2KCl+3O2↑這個過程中高錳酸鉀轉化為二氧化錳的等物質,其中的二氧化錳改變了氯酸鉀的分解速率,所以作催化劑的是二氧化錳,而非高錳酸鉀.從概念的角度,催化劑是質量和化學性質都不改變的物質,在這里,高錳酸鉀分解了,那么本身的化學性質改變,自身分解了,質量當然也就發生了改變,即高錳酸鉀在反應前后質量和化學性質都發生了改變.所以高錳酸鉀不是該反應的催化劑.
